Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
笹岡 香織*; 片岡 隆浩*; 神崎 訓枝; 小橋 佑介*; 迫田 晃弘; 石森 有; 山岡 聖典*
Pakistan Journal of Zoology, 50(3), p.1157 - 1170, 2018/06
被引用回数:2 パーセンタイル:17.52(Zoology)シスプラチン(CDDP)は固形がんの治療に広く使用されているが、酸化ストレスによる腎毒性を持っている。そこで、我々は、ラドン吸入による放射線感受性の違いによるマウス系統差によるCDDP誘導腎障害に対する影響とCDDP濃度について検討した。まず、C57BL/6JまたはBALB/cのマウスに、1000Bq/m または2000Bq/m
または2000Bq/m のラドンを24時間吸入後、CDDPを20mg/kg体重投与した。C57BL/6Jでは毛並等が改善され、BALB/cでは悪化した。次に、BALB/cマウスに、1000Bq/m
のラドンを24時間吸入後、CDDPを20mg/kg体重投与した。C57BL/6Jでは毛並等が改善され、BALB/cでは悪化した。次に、BALB/cマウスに、1000Bq/m のラドンを24時間後、CDDPを15mg/kg体重投与した。その結果、抗酸化機能の亢進などが見られた。以上のことから、ラドン吸入によってCDDP誘導腎障害を抑制することが可能であることが示唆された。
のラドンを24時間後、CDDPを15mg/kg体重投与した。その結果、抗酸化機能の亢進などが見られた。以上のことから、ラドン吸入によってCDDP誘導腎障害を抑制することが可能であることが示唆された。
吉田 勝; 浅野 雅春; 森田 泰司*; 嘉悦 勲; 今井 強一*; 真下 透*; 湯浅 久子*; 山中 英寿*; 河原田 うめ子*; 鈴木 慶二*
Biomaterials, 10, p.16 - 22, 1989/01
被引用回数:10 パーセンタイル:46.07(Engineering, Biomedical)シスプラチンを低温放射線重合法によってビニルコポリマー(80/20vol-%組成のdiethylene glycol dimethacrylate/polyethylene glycol #600 dimethacrylate)中に固定した。
吉田 勝; 浅野 雅春; 嘉悦 勲; 今井 強一*; 真下 透*; 湯浅 久子*; 山中 英寿*; 鈴木 慶二*; 森田 泰司*
人工臓器, 16(3), p.1333 - 1336, 1987/03
低温放射線重合法で調製したシスプラチンを含むvinyl copolymer針をウィスター系ラットの腎臓に埋入した。この針からシスプラチンが徐々に放出され、結果的に針周囲・組織が壊死化した。針周囲の組織壊死の立体像はラグビーボール状で、その中心に針が位置している形態を示した。この場合、針表面から外側へ向っての壊死の組織形態は凝固壊死層、融解壊死層そして非壊死(正常組織)からなることが分った。このような組織形態はurokinase(フィブリン溶融酵素)、lipase(脂肪分解酵素)およびtrypsin(タンパク質分解酵素)のような酵素をシスプラチンと共存させた時に顕著に変化した。すなわち、針埋入から7日目で比較した場合、非酵素もしくはurokinase含有系の壊死形態は殆んどが凝固壊死であったのに対し、lipaseおよびtrypsin含有系のそれは逆に融解壊死からなっていることが組織所見(HE染色)から判明した。
吉田 勝
医学のあゆみ, 136(12), p.917 - 920, 1986/00
「医学のあゆみ」の講座に掲載予定の論文で、その内容は、高分子材料からの制癌剤のin vivo放出パターンによって組織壊死作用がどの程度の範囲に及ぶのかを埋入期間を関数として評価した研究成果からなる。制癌剤は主に白金化合物のシスプラチンを、そして高分子材料は生体分解型のcopoly(DL-alanine/ -ethyl-L-aspartate,75/25mol-%)と生体非分解型のcopoly(diethlen glycol dimethacrylate/polyethlene glycol #600 dimethacrylate,80/20 vol-%)を使用する。シスプラチン除放性針は低温放射線注形重合法もしくは加圧-加熱溶解法によって調整し、いずれも1.6mm径,5mm長さの高密度・高剛性の性質をもつ複合体である。この複合体からのシスプラチンの放出パターンはSEMとXMAによって検討する。
-ethyl-L-aspartate,75/25mol-%)と生体非分解型のcopoly(diethlen glycol dimethacrylate/polyethlene glycol #600 dimethacrylate,80/20 vol-%)を使用する。シスプラチン除放性針は低温放射線注形重合法もしくは加圧-加熱溶解法によって調整し、いずれも1.6mm径,5mm長さの高密度・高剛性の性質をもつ複合体である。この複合体からのシスプラチンの放出パターンはSEMとXMAによって検討する。
嘉悦 勲; 吉田 勝; 浅野 雅春; 久保 長生*; 喜多村 孝一*; 今井 強一*; 真下 透*; 湯浅 久子*; 山中 英寿*; 鈴木 慶二*
人工臓器, 15(1), p.214 - 217, 1986/00
低温放射線重合法によってnonbiodegrable vinyl copolymer中に制癌剤を包含し、徐放性針状複合体(1.6mm径、5mm長)を調製した。cisplatinを含む複合体針をウィスター系ラットの腎臓に7日間にわたって埋入留置した時、制癌剤のin vivo累積放出量は仕込みの12%であった。この値は複合体針の埋入箇所の違いによって著明に異なった。例えば、cisplatinのin vivo累積放出量は皮下埋入に対し38%、肝臓埋入に対し21%そして脳埋入に対し7%を示した。一方、徐放性制癌剤による組織壊死範囲は制癌剤の種類によって著しく異なり、例えば腎臓に対する壊死の場合、その作用はcisplain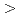 MMC
MMC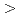 ADM
ADM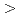 ACNU
ACNU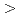 5-FUの順に減少した。しかし、脳の場合、組織の壊死作用はACNUの方がcisplatinより顕著に有効であった。従って、組織の違いによっても、徐放性制癌剤の壊死作用が異なることが結論できた。これらの結果に基づいて、ACNU含有複合体針を中心に脳腫瘍領域に適用を試みた。
5-FUの順に減少した。しかし、脳の場合、組織の壊死作用はACNUの方がcisplatinより顕著に有効であった。従って、組織の違いによっても、徐放性制癌剤の壊死作用が異なることが結論できた。これらの結果に基づいて、ACNU含有複合体針を中心に脳腫瘍領域に適用を試みた。
吉田 勝; 浅野 雅春; 嘉悦 勲; 今井 強一*; 真下 透*; 湯浅 久子*; 山中 英寿*; 久保 長生*
人工臓器, 14(2), p.830 - 833, 1985/00
放射線重合法・加圧加熱溶融法によってポリマー担体(7mg)中に制癌剤(5mg)を包含し、除放性機能と局所療法を目的とする種々の針状複合体を調製した。この複合体をラットの正常肝臓に挿入し薬物拡散と組織壊死の範囲をコントロールすることを目標として、その壊死状態を検討した。cisplatinを含む生体分解copoly(DL-alanine/ -ethyl-L-aspartate,75/25)を用いた時に最大壊死範囲(14mm径)が観察された。この場合、組織壊死は複合体挿入から3日目で最大に達した。複合体からの制癌剤の放出パターンが微量長期放出および多量短期放出タイプの場合、組織壊死は上記の範囲より著しく狭くなった。従って、肝臓組織を広範囲に壊死化するには、複合体からの制癌剤のin vivo放出は試験開始から3日程度の期間に集中させ、この期間に仕込み制癌剤量の90%以上を放出させるような複合体系が望ましいと結論した。
-ethyl-L-aspartate,75/25)を用いた時に最大壊死範囲(14mm径)が観察された。この場合、組織壊死は複合体挿入から3日目で最大に達した。複合体からの制癌剤の放出パターンが微量長期放出および多量短期放出タイプの場合、組織壊死は上記の範囲より著しく狭くなった。従って、肝臓組織を広範囲に壊死化するには、複合体からの制癌剤のin vivo放出は試験開始から3日程度の期間に集中させ、この期間に仕込み制癌剤量の90%以上を放出させるような複合体系が望ましいと結論した。